Коперниций — самый тяжёлый элемент периодической таблицы Менделеева
Металлы человечество начало активно использовать еще в 3000-4000 годах до нашей эры. Тогда люди познакомились с самыми распространенными из них, это золото, серебро, медь. Эти металлы было очень легко найти на поверхности земли. Чуть позже они познали химию и начали выделять из них такие виды как олово, свинец и железо. В Средневековье набирали популярность очень ядовитые виды металлов. В обиходе был мышьяк, которым было отравлено больше половины королевского двора во Франции. Так же и ртуть, которая помогала вылечить разные болезни тех времен, начиная от ангины и до чумы. Уже до двадцатого столетия было известно более 60 металлов, а вначале XXI века – 90. Прогресс не стоит на месте и ведет человечество вперед. Но встает вопрос, какой металл является тяжелым и превосходит по весу все остальные? И вообще, какие они, эти самые тяжелые металлы в мире?
Многие ошибочно думают, что золото и свинец являются самыми тяжелыми металлами. Почему именно так сложилось? Многие из нас выросли на старых фильмах и видели, как главный герой использует свинцовую пластину для зашиты от злобных пуль. В добавок, и сегодня используют свинцовые пластины в некоторых видах бронежилетов. А при слове золото у многих всплывает картинка с тяжелыми слитками этого металла. Но думать, что они самые тяжелые – ошибочно!
Для определения самого тяжелого металла надо брать во внимание его плотность, ведь чем больше плотность вещества, тем оно тяжелее.
Общая информация
На протяжении веков люди занимались изучением полезных свойств самых распространенных металлов на планете. Больше всего сведений наука хранит о золоте серебре и меди. Со временем человечество познакомилось с железом, более легкими металлами – оловом и свинцом. В мире Средневековья люди активно пользовались мышьяком, а болезни лечили ртутью.
Благодаря стремительному прогрессу, сегодня самыми тяжелыми и плотными металлами считается не один элемент таблицы, а сразу два. Под номером 76 расположен осмий (Os), а под номером 77 – иридий (Ir), вещества имеют следующие показатели плотности:
- осмий тяжелый, благодаря плотности 22,62 г/ см³;
- иридий не намного легче – 22,53 г/ см³.
Плотность относят к физическим свойствам металлов, она представляет собой соотношение массы вещества к его объему. Теоретические расчеты плотности обоих элементов имеют некоторые погрешности, поэтому оба металла сегодня принято считать самыми тяжелыми.
Для наглядности можно сравнить вес обыкновенной пробки с весом пробки из самого тяжелого металла в мире. Чтобы уравновесить чаши весов с пробкой из осмия либо иридия, потребуется более сотни обычных пробок.
Серебро
Серебро, как и золото известно человечеству с давних времен. Оно используется не только при изготовлении ювелирных украшений, но и для производства посуды. Ранее серебро очень активно использовали при чеканке монет. И сегодня можно увидеть некоторые монеты, содержащие в себе немного серебра. При выборе драгоценного металла, нередко возникает вопрос, что же все-таки тяжелее золото или же другой драгоценный металл — серебро.
Плотность этого металла немного меньше, чем плотность свинца. Она равна 10,5 грамм на сантиметр кубический. Это говорит о том, что золото тяжелее серебра почти в два раза.
Кроме создания столового серебра и различных украшений, этот материал очень активно используют в промышленности, а также в сфере фотоиндустрии.

Основными свойствами, благодаря которым этот элемент стал так широко применяться в промышленной сфере, являются отличная тепло- и электропроводность, отличная устойчивость к взаимодействию с окружающей средой, а также превосходные отражающие способности.
Быстро развивающийся технический прогресс заметно сократил использование серебра в фотоиндустрии. Это связано с тем, что благодаря внедрению современных технологий процесс производства и использования фототехники стал намного доступнее для большинства людей. Именно это и обеспечило сокращение использования серебра более чем в 3 раза.
Благодаря своим бактерицидным свойствам этот металл очень активно используется в медицине. В данный момент серебро используют для производства антибактериального пластыря, а также производства фильтров для очистки воды от вредных микроорганизмов.

Нитрат серебра, используемый в медицине.
История открытия металлов
Оба элемента были открыты на заре XIX века ученым Смитсоном Теннантом. Многие исследователи того времени занимались изучением свойств сырой платины, обрабатывая ее «царской водкой». Только Теннанту удалось обнаружить в полученном осадке два химических вещества:
- осадочный элемент со стойким запахом хлора ученый назвал осмием;
- субстанция с меняющейся окраской получила название иридий (радуга).
Оба элемента были представлены единым сплавом, который ученому удалось разделить. Дальнейшим исследованием самородков платины занялся русский химик К. Клаус, тщательно исследовавший свойства осадочных элементов. Сложность определения самого тяжелого металла в мире заключается в невысокой разности их плотности, которая не является величиной постоянной.

Читайте также: Где больше всего км конденсаторов. Конденсатор: применение и виды. Чем являются КМ-конденсаторы











Тантал, Плотность: 16,69 г/см3
Тантал относится к тугоплавкой группе металлов, которая составляет незначительную долю в различных типах сплавов. Он твердый, редкий и обладает высокой устойчивостью к коррозии, что делает его идеальным материалом для высокопроизводительных конденсаторов, которые идеально подходят для домашних компьютеров и электроники.
Другое важное применение тантала — в хирургических инструментах и в имплантатах тела из-за его способности непосредственно связываться с твердыми тканями внутри нашего тела.
Яркие характеристики самых плотных металлов
Добытые экспериментальным путем вещества представляют собой порошок, довольно трудно поддающийся обработке, ковка металлов требует очень высоких температур. Наиболее распространенной формой содружества иридия с осмием является сплав осмистого иридия, который добывают в месторождениях платины, пластах залегания золота.
Наиболее частым местом обнаружения иридия считаются метеориты, богатые железом. Самородного осмия в мире природы не найти, только в содружестве с иридием и другими компонентами платиновой группы. Залежи часто содержат соединения серы с мышьяком.
Особенности самого тяжелого и дорогого металла в мире
Среди элементов периодической таблицы Менделеева самым дорогостоящим считается осмий. Серебристый металл с голубоватым отливом принадлежит к платиновой группе благородных химических соединений. Свой блеск самый плотный, но очень хрупкий металл не теряет под воздействием высоких температурных показателей.

Характеристики
- Элемент №76 Osmium имеет атомную массу 190,23 а.е.м.;
- Расплавленное при температуре 3033°C вещество закипит при 5012°C.
- Самый тяжелый материал обладает плотностью 22,62 г/ см³;
- Структура кристаллической решетки имеет гексагональную форму.
Несмотря на изумительно холодный блеск серебристого отлива, осмий не годится для производства ювелирных изделий из-за высочайшей токсичности. Для плавки украшения потребовалась бы температура, как на поверхности Солнца, ведь самый плотный в мире металл разрушается при механическом воздействии.
Превращаясь в порошок, осмий взаимодействует с кислородом, реагирует на серу, фосфор, селен, на царскую водку реакция вещества очень медленная. Osmium не обладает магнетизмом, сплавы имеют склонность к окислению, формированию кластерных соединений.

Где применяют
Самый тяжелый и невероятно плотный металл обладает высокой износостойкостью, поэтому добавка его к сплавам значительно повышает их крепость. Применение осмия в основном связано с химической промышленностью. Кроме того, его используют для следующих нужд:
- изготовления ёмкостей, предназначенных для хранения отходов ядерного синтеза;
- для нужд ракетостроения, оружейного производства (боеголовки);
- в часовой промышленности для изготовления механизмов брендовых моделей;
- для изготовления хирургических имплантатов, деталей кардиостимуляторов.
Интересно, что самый плотный металл считается единственным в мире элементом, неподвластным воздействию агрессии «адской» смеси кислот (азотная и соляная). Алюминий, соединенный с осмием, становится настолько пластичным, что его можно вытягивать без разрыва.
Тайны самого редкого и плотного в мире металла
Принадлежность иридия к платиновой группе наделяет его свойством невосприимчивости к обработке кислотами и их смесями. В мире иридий получают из анодных шламов при медно-никелевом производстве. После обработки шлама царской водкой, выпавший осадок прокаливают, результатом чего становится добыча иридия.

Характеристики
Самый твердый металл серебристо-белого цвета обладает следующей группой свойств:
- элемент таблицы Менделеева Iridium №77 обладает атомной массой 192,22 а.е.м.;
- расплавленное при температуре 2466°C вещество закипит при 4428°C;
- плотность расплавленного иридия – в пределах 19,39 г/см³;
- плотность элемента при комнатной температуре – 22,7 г/см³;
- кристаллическая решётка иридия ассоциируется с гранецентрированным кубом.
Тяжелый иридий не меняется под воздействием обычной температуры воздуха. Результатом прокаливания под воздействием нагревания при определенных температурах становится образование многовалентных соединений. Порошок свежего осадка иридиевой черни поддается частичному растворению царской водкой, а также раствором хлора.

Область применения
Хотя Iridium принадлежит к числу драгоценных металлов, для ювелирных изделий его применяют редко. Элемент, плохо поддающийся обработкам, весьма востребован при строительстве дорог, производстве автомобильных деталей. Сплавы с неподверженным окислению самым плотным металлом применяются для следующих целей:
- изготовления тиглей для проведения лабораторных опытов;
- производства специальных мундштуков для стеклодувов;
- покрытия кончиков перьев и стержней шариковых ручек;
- изготовления долговечных свечей зажигания для автомобилей;
Сплавы с изотопами иридия используют на сварочном производстве, в приборостроении, для выращивания кристаллов в составе лазерной техники. Применение самого тяжелого металла позволило осуществлять лазерную коррекцию зрения, дробление камней в почках и другие медицинские процедуры.
Хотя Iridium лишен токсичности и не опасен для биологических организмов, в природной среде можно встретиться его опасным изотопом – гексафторидом. Вдыхание паров ядовитого вещества ведет к мгновенному удушью и смерти.
Рений, Плотность :21,2 г/см 3
Элемент Рений назван в честь реки Рейн в Германии после того, как он был обнаружен тремя немецкими учеными в начале 1900-х годов. Как и другие металлы платиновой группы, рений также является драгоценным элементом Земли и имеет вторую самую высокую температуру кипения, третью самую высокую температуру плавления любого известного элемента на Земле.
Из-за таких экстремальных свойств рений (в виде суперсплавов) широко используется в лопатках турбин и движущихся соплах практически всех реактивных двигателей во всем мире. Это также один из лучших катализаторов риформинга нафты (жидкой углеводородной смеси), изомеризации и гидрирования.
Места природного залегания
Залежи самого плотного металла Iridium в мире природы ничтожно малы, их намного меньше, чем запасов платины. Предположительно самое тяжелое вещество сместилось к ядру планеты, поэтому объемы промышленной добычи элемента невелики (около трех тонн в год). Изделия из сплавов с иридием могут прослужить до 200 лет, драгоценности станут более долговечными.

Самородков самого тяжелого металла с неприятным запахом Osmium в природе не найти. В составе минералов можно обнаружить следы осмистого иридия вместе с платиной и палладием, рутением. Залежи осмистого иридия разведаны на территории Сибири (Россия), некоторых штатов Америки (Аляска и Калифорния), в Австралии и Южной Африке.
Если обнаружены залежи платины, удастся выделить осмий с иридием для укрепления и усиления физических либо химических соединений различных изделий.
Платина, Плотность: 21,45 г/см3
Платина является чрезвычайно редким металлом на Земле со средним содержанием 5 микрограммов на килограмм. Южная Африка является крупнейшим производителем платины с 80% мирового производства, а также небольшим вкладом США и России. Это плотный, пластичный и нереактивный металл.
Помимо символа престижа (ювелирные изделия или любые аналогичные аксессуары), платина используется в различных областях, таких как автомобильная промышленность, где она используется для производства устройств контроля выбросов автомобилей и для переработки нефти. Другие малые области применения включают, например, медицину и биомедицину, оборудование для производства стекла, электроды, противоопухолевые препараты, датчики кислорода, свечи зажигания.
Свинец
Следует сказать, что плотность свинца почти в 10 раз меньше плотности благородного желтого металла. Чтобы осознать плотность свинца, следует сказать о том, что плотность березы или липы в 25 раз меньше. По таблице плотностей, свинец находится на 20 месте, а золото на седьмом. Из этого несложно сделать вывод о том, что желтый металл намного тяжелее своего оппонента.

Данный элемент очень хорошо используется в производстве различных конструкций из металла, а также в медицинской сфере. Это связано с непропусканием лучей рентгеновского излучения. Широкое применение свинца в различных сферах связано еще с очень дешевой стоимостью этого металла. Его стоимость практически в два раза меньше стоимости алюминия. Еще одним плюсом выступает относительная легкость добычи данного материала, это обеспечивает огромное поступления предложения на мировой рынок.
ЗОЛОТО
ЗОЛОТО – элемент группы IА периодической таблицы. Благодаря малой химической активности относится к так называемым благородным металлам. В природе представлен единственным стабильным нуклидом 197 Au. Искусственно получено более десяти радиоактивных изотопов золота, из которых самый долгоживущий – 195 Au с периодом полураспада 183 сут. С древнейших времен блеск золота сопоставлялся с блеском солнца (на латыни – sol), отсюда и русское «золото». Английское и немецкое слово gold, голландское goud, шведское и датское guld (отсюда, кстати, гульдены) в европейских языках связаны с индоевропейским корнем ghel и даже с греческим богом солнца Гелиосом. Латинское название золота aurum означает «желтое» и родственно с Авророй (Aurora) – утренней зарей.
У алхимиков золото считалось «царем металлов», его символом было лучезарное солнце, а символом серебра – луна (при этом отношение цены золота и серебра в Древнем Египте соответствовало отношению солнечного года к лунному месяцу).
Золото в природе.
Золота в земной коре очень мало: всего 4,3·10 –7 % по массе, т.е., в среднем, лишь 4 мг в тонне горных пород, это один из самых редких элементов: его втрое меньше редкого металла палладия, в 15 раз меньше серебра, в 300 раз меньше вольфрама, в 600 раз меньше урана, в 10 тысяч раз меньше меди. Если бы все золото было равномерно рассеяно – как в морской воде – его добыча была бы невозможна (см. ГАБЕР). Однако золото способно активно мигрировать, например, с подземными водами, в которых растворен кислород. В результате различных миграционных процессов золото концентрируется в месторождениях – в кварцевых золотоносных жилах, в золотоносном песке.
Различают рудное и россыпное золото. Рудное золото встречается в виде вкрапленных в кварц мелких (от 0,0001 до 1 мм) золотинок, в таком виде оно встречается в кварцевых породах в форме тонких включений или более мощных жил, пронизывающих сульфидные руды – серный колчедан FeS2, медный колчедан CuFeS2, сурьмяный блеск Sb2S3 и др. Другая форма рудного золота – его довольно редкие минералы, в которых золото находится в виде химических соединений (чаще всего – с теллуром, с которым образует серебристо-белые кристаллы, иногда с желтым оттенком): калаверит AuTe2, монтбрейит Au2Te3, мутманнит (Ag,Au)Te (скобки указывают, что эти элементы могут содержаться в минерале в разных пропорциях), креннерит (Ag,Au)Te2, сильванит (Ag,Au)2Te4, монтбрейит (Au,Sb)2Te3, петцит Ag3AuTe2, ауростибит AuSb2, аурантимонат AuSbO3, аурикуприд Cu3Au, нагиагит Pb5Au(Te,Sb)4S5–8, тетрааурикуприд AuCu, фишессерит Ag3AuSe2 и другие.
Часть золота в процессах геологических изменений уносилась из мест первичного залегания и вновь откладывалась в местах вторичного залегания, так образовалось россыпное золото – продукт разрушения коренных месторождений, которые накапливались в долинах рек. В нем изредка находят большие самородки, порой причудливой формы. Некоторые такие месторождения образовались 20 – 30 тысяч лет назад. Самое же богатое на Земле месторождение, которое тянется вдоль горной гряды Витватерсранд (в переводе с голландского «Край белой воды») в Южной Африке, очень старое – ему около 3 млрд. лет.
Самородное золото – не химически чистое золото, в нем всегда есть примеси, иногда – в значительном количестве: серебро (от 2 до 50%), медь (до 20%), железо, ртуть, металлы платиновой группы, висмут, свинец, теллур и другие. Природный сплав золота с серебром, содержащий 15 – 30% серебра и немного меди, древние греки называли электроном (римляне – электрумом) за его желтый цвет: по-гречески elektor – лучезарное светило, солнце, отсюда и греч. elektron – янтарь.
Сравнительно высокая концентрация золота найдена в воде горячих источников. Так, в Новой Зеландии отложения золота были обнаружены в трубах электростанции, работающей на гидротермальных водах. Мигрируя с почвенными водами, золото попадает и в растения, некоторые из них (хвощи, кукуруза) способны собирать золото. Зола хвощей в золотоносных районах может содержать до 0,065% драгоценного металла. Собирать золото могут и некоторые бактерии, осаждая его из разбавленных растворов.
Физические свойства.
Золото – один из самых тяжелых металлов: его плотность 19,3 г/см 3 . Тяжелее золота только осмий, иридий, платина и рений. На одной из выставок демонстрировался небольшой полированный золотой кубик размером чуть больше 5 см, причем объявление гласило, что тот, кто сможет поднять его двумя пальцами одной руки, может унести его с собой. Организаторы ничем не рисковали: никакой силач не смог бы поднять таким образом скользкий слиток, весящий несколько килограммов. Если плотно заполнить золотыми слитками комнату площадью 20 кв.м и высотой 3 м, их масса составит 1150 т – вес тяжело груженного железнодорожного состава.
«Чистое золото отражает желтый свет, а в виде очень тонких листов (листовое золото), в которые оно способно выковываться и вытягиваться, просвечивает синевато-зеленым цветом. При нагревании даже в горнах золото дает пары, отчего пламя, проходящее над ним, окрашивается в зеленоватый цвет» (Д.И.Менделеев. Основы химии).
Желтый цвет имеет химически чистое золото, однако примеси могут окрашивать его в другие цвета – от белого до зеленого. Червонный (красный) цвет придает золоту, например, медь при определенном ее содержании в сплаве. Так, в изданной в 1905 энциклопедии под редакцией Ю.Н.Южакова сказано: «Червонное золото – сплав золота с медью в отношении 9:1, употребляется для чеканки монет». О том же говорит и словарь В.И.Даля: «Красное золото – с медным сплавом; белое золото – с серебряным сплавом».
Золото – сравнительно легкоплавкий металл, плавится при 1064° С, кипит при 2880° С, по теплопроводности и электропроводности занимает третье место (после серебра и меди). Твердость золота по 10-балльной шкале Мооса составляет всего 2,5, чистое золото слишком мягкое и не годится ни для каких изделий. Для твердости к нему всегда добавляют другие металлы, например, серебро или медь (см. ЗОЛОТЫЕ ИЗДЕЛИЯ).
Золото легко сплавляется со многими металлами, которые могут входить в кристаллическую структуру золота, не нарушая ее, а просто замещая атомы золота. В таком случае образуются твердые растворы. Природные твердые растворы с золотом могут образовывать серебро, медь, платина, палладий, родий, иридий, ряд других металлов, размеры атомов которых такие же, как у золота (радиус 0,14 нм) или очень мало от него отличаются. Твердые природные растворы Au–Ag иногда содержат до 10% ртути (например, в месторождении Золотая гора на Урале). В присутствии примеси железа (некоторые находки в Якутии содержат до 4,45% Fe) минерал становится магнитным.
Химические свойства.
За прошедшие столетия химики (а до них алхимики) провели с золотом огромное количество различных экспериментов, и оказалось, что золото вовсе не так инертно, как об этом думают неспециалисты. Правда, сера и кислород (агрессивные по отношению к большинству металлов, особенно при нагревании), на золото не действуют ни при какой температуре. Исключение – атомы золота на поверхности. При 500–700° С они образуют чрезвычайно тонкий, но очень устойчивый оксид, не разлагающийся в течение 12 часов при нагреве до 800° С. Это может быть Au2O3 или AuO(OH). Такой оксидный слой найден на поверхности крупинок самородного золота.
Не реагирует золото и с водородом, азотом, фосфором, углеродом, а галогены с золотом при нагревании реагируют с образованием AuF3, AuCl3, AuBr3 и AuI. Особенно легко, уже при комнатной температуре идет реакция с хлорной и бромной водой. С этими реактивами встречаются только химики. В быту опасность для золотых колец представляет иодная настойка – водно-спиртовый раствор иода и иодида калия: 2Au + I2 + 2KI ® 2K[AuI2].
Щелочи и большинство минеральных кислот на золото не действуют. Но смесь концентрированных азотной и соляной кислот («царская водка») легко растворяет золото: Au + HNO3 + 4HCl ® H[AuCl4] + NO + 2H2O. После осторожного выпаривания раствора выделяются желтые кристаллы комплексной золотохлористоводородной кислоты HAuCl4 ·3H2O. Царскую водку, способную растворять золото, знал еще арабский алхимик Гебер, живший в 9–10 вв. Менее известно, что золото растворяется в горячей концентрированной селеновой кислоте: 2Au + 6H2SeO4 ® Au2(SeO4)3 + 3H2SeO3 + 3H2O. В концентрированной серной кислоте золото растворяется в присутствии окислителей: иодной кислоты, азотной кислоты, диоксида марганца. В водных растворах цианидов при доступе кислорода золото растворяется с образованием очень прочных дицианоауратов: 4Au + 8NaCN + 2H2O + O2 ® 4Na[Au(CN)2] + 4NaOH; эта реакция лежит в основе важного промышленного способа извлечения золота из руд. Действуют на золото и расплавы из смеси щелочей и нитратов щелочных металлов: 2Au + 2NaOH + 3NaNO3 ® 2Na[AuO2] + 2Na2O, пероксиды натрия или бария: 2Au + 3BaO2 ® Ba[AuO2]2 + 3BaO, водные или эфирные растворы высших хлоридов марганца, кобальта и никеля: 3Au + 3MnCl4 ® 2AuCl3 + 3MnCl2, тионилхлорид: 2Au + 4SOCl2 ® 2AuCl3 + 2SO2 + S2Cl2, некоторые другие реагенты. Итак, золото далеко не так «благородно», как это принято считать.
Интересны свойства мелкораздробленного золота. При восстановлении золота из сильно разбавленных растворов оно не выпадает в осадок, а образует интенсивно окрашенные коллоидные растворы – гидрозоли, которые могут быть пурпурно-красными, синими, фиолетовыми, коричневыми и даже черными. Так, при добавлении к 0,0075%-ному раствору H[AuCl4] восстановителя (например, 0,005%-ного раствора солянокислого гидразина) образуется прозрачный голубой золь золота, а если к 0,0025%-ному раствору H[AuCl4] добавить 0,005%-ный раствор карбоната калия, а затем по каплям при нагревании добавить раствор танина, то образуется красный прозрачный золь. Таким образом, в зависимости от степени дисперсности окраска золота меняется от голубой (грубодисперсный золь) до красной (тонкодисперсный золь). При размере частиц золя 40 нм максимум его оптического поглощения приходится на 510–520 нм (раствор красный), а при увеличении размера частиц до 86 нм максимум сдвигается до 620–630 нм (раствор голубой). Реакция восстановления с образованием коллоидных частиц используется в аналитической химии для обнаружения малых количеств золота.
При восстановлении растворов соединений золота хлоридом олова(II) в слабокислых растворах образуется интенсивно окрашенный темно-пурпурный раствор так называемого кассиевого золотого пурпура (он назван так по имени Андреаса Кассия, стекловара из Гамбурга, жившего в 17 в.). Это очень чувствительная реакция. Когда золотой золь теряет устойчивость (коагулирует), образуется черный осадок, т.к. что именно такой цвет имеет порошок любого металла в тонкодисперсном состоянии. Кассиев пурпур, введенный в расплавленную стеклянную массу, дает великолепно окрашенное рубиновое стекло, количество затрачиваемого при этом золота ничтожно. Кассиев пурпур применяется и для живописи по стеклу и фарфору, давая при прокаливания различные оттенки – от слаборозового до ярко-красного.
Известны и органические соединения золота. Так, действием хлорида золота(III) на ароматические соединения получают соединения, устойчивые к воде, кислороду и кислотам, например: AuCl3 + C6H6 ® C6H5AuCl2 + HCl. Органические производные золота(I) стабильны только в присутствии координационно связанных с золотом лигандов, например, триэтилфосфина: CH3Au·P(C2H5)3.
Добыча золота: технология.
В результате природного концентрирования примерно лишь 0,1% всего золота, содержащегося в земной коре, доступна, хотя бы теоретически, для добычи, однако благодаря тому, что золото встречается в самородном виде, ярко блестит и легко заметно, оно стало первым металлом, с которым познакомился человек. Но природные самородки редки, поэтому самый древний способ добычи редкого металла, основанный на большой плотности золота, – промывание золотоносных песков. «Добыча. промывного золота требует только механических средств, а потому немудрено, что золото известно было даже дикарям и в самые древние исторические времена» (Д.И.Менделеев. Основы химии).
«Дикари» встряхивали золотоносный песок в потоке воды на наклонном лотке, при этом более легкий песок смывается, а золотые крупинки остаются на лотке. Такой способ применяли старатели и в новейшее время. Золото почти в 20 раз тяжелее воды и примерно в 8 раз тяжелее песка, поэтому крупинки золота можно струей воды отделить от песка или от измельченной пустой породы. Старинный способ промывки с помощью бараньих шкур, на которых отлагались золотые крупинки, отражен в древнегреческом мифе о золотом руне. Самородки и россыпи золота часто находили по течению рек, которые тысячелетиями размывали золотоносные породы. В древние времена золото добывали только из россыпей, и сейчас там, где они остались, золотоносный песок вычерпывают со дна рек и озер и обогащают на драгах – огромных сооружениях размером с многоэтажный дом, способных перерабатывать миллионы тонн золотоносной породы в год. Но богатых золотых россыпей почти не осталось, и уже в начале 20 в. 90% всего золота добывали из руд. Сейчас многие золотые россыпи практически исчерпаны, поэтому добывают, в основном, рудное золото, правда, теперь добыча рудного золота во многом механизирована, но остается трудным производством, часто спрятанным глубоко под землей. В последние десятилетия постоянно росла доля более рентабельных открытых разработок. Месторождение экономически выгодно разрабатывать, если в тонне руды содержится всего 2–3 г золота, а при содержании более 10 г/т оно считается богатым. Существенно, что затраты на поиск и разведку новых золотых месторождений составляют от 50 до 80% всех затрат на геологоразведочные работы.

Старый (так называемый ртутный) способ извлечения золота из руды – амальгамирование основан на том, что ртуть хорошо смачивает (но практически не растворяет) золото – как вода смачивает (но не растворяет) стекло. Тонко размолотую золотоносную породу встряхивали в бочках, на дне которых находилась ртуть. При этом частички золота прилипали к жидкому металлу, смачиваясь ртутью со всех сторон. Поскольку при этом цвет золотых частиц исчезает, может показаться, что золото «растворилось». Затем ртуть отделяли от пустой породы и сильно нагревали. Летучая ртуть отгонялась, а золото оставалось в неизменном виде. Недостатки этого метода – высокая ядовитость ртути и неполнота выделения золота: самые мелкие его частицы смачиваются ртутью плохо.
В романе А.Н.Толстого Гиперболоид инженера Гарина герой надеется разбогатеть, найдя в глубинах земного шара «золотой слой» из жидкого «ртутного золота», содержащего «девяносто процентов червонного золота». Его предполагалось «черпать прямо с поверхности» и по трубопроводам перекачивать в печи, где должны были получить чистое золото, испаряя ртуть. На самом деле истинная растворимость золота в ртути очень мала и составляет всего 0,126% при 20° С. При длительном выдерживании золота в ртути идет химическая реакция с образованием твердых при комнатной температуре интерметаллических соединений состава AuHg2, Au2Hg и Au3Hg, а при высоком содержании золота возможно также образование его твердых растворов с ртутью. Ни химические соединения, ни твердые растворы золота и ртути нельзя ни «черпать с поверхности», ни пропускать по «ртутопроводу», как предполагал делать Гарин.
Более современный способ добычи золота из бедных руд – выщелачивание цианидом натрия, при котором даже самые мелкие крупинки переводят в водорастворимые цианистые соединения. Затем из водного раствора извлекают золото, например, извлекая его с помощью цинкового порошка: 2Na[Au(CN)2] + Zn ® Na[Zn(CN)4] + 2Au. Выщелачивание позволяет извлекать остатки золота из отвалов заброшенных разработок, фактически превращая их в новое месторождение. Перспективен и метод подземного выщелачивания: раствор цианида закачивают в скважины, он по трещинам проникает внутрь породы, где растворяет золото, после чего раствор выкачивают через другие скважины. Конечно, цианид будет переводить в раствор не только золото, но и другие металлы, образующие устойчивые цианидные комплексы.
Другой, довольно бедный, но постоянный источник золота, – промежуточные продукты свинцово-цинкового, медного, уранового и некоторых других производств. Оно основано на том, что золото нередко соседствует с другими металлами. В полиметаллических рудах золото часто содержится в виде небольшой примеси, и процесс их переработки стараются вести так, чтобы попутно извлекать и золото, если это оказывается рентабельным. Так, при электролитической очистке (рафинировании) меди, когда ее «перегоняют» с анода на катод, благородные металлы при растворении анода не переходят в раствор, а скапливаются под анодом в виде ила (шлама). Этот шлам – важный источник получения золота, которого добывают тем больше, чем более масштабно производство основных металлов. Например, в США это один из основных источников золота.
Так называемое вторичное золото получают из огромной массы отработавших или бракованных изделий электроники. Их прямо в нераспакованных ящиках бросают в расплавленную медь; дерево моментально сгорает, алюминий, железо, олово, другие неблагородные металлы переходят в оксиды, всплывают на поверхность расплава и удаляются, а медь после достаточного обогащения благородными металлами направляют на рафинирование. Важный источник вторичного золота (до 500 т) в год – золотой лом.
И лишь теоретический интерес представляют ядерные реакции, с помощью которых из неблагородных металлов можно получить «алхимическое золото». Примером может служить гипотетическая реакция 209 Bi + 32 S ® 197 Au + 44 Ca, а также наблюдавшаяся реакция захвата одного «своего» электрона из К-оболочки (К-захват) атомом одного из радиоактивных изотопов ртути: 197 Hg + e ® 197 Au.
Добыча золота: мировое производство.
Самые старые из известных историкам золотых приисков находились в Египте. Есть данные о добыче золота и изготовлении из него различных изделий еще в пятом тысячелетии до н.э. – в каменном веке. Скалы с золотоносными кварцевыми жилами раскаляли в огне, а затем обливали холодной водой. Растрескавшуюся породу измельчали – дробили, толкли в ступах, мололи и подвергали промывке. Древние египтяне добывали золото в Аравийско-Нубийской золотоносной провинции, расположенной между Нилом и Красным морем. За много веков, на протяжении царствования 30 династий она дала его огромное количество – порядка 3500 тонн. Так, только при фараоне Тутмосе III, ежегодная добыча доходила до 50 т. Одно время для добывания золота там затрачивалось меньше труда, чем для других металлов, и золото стоило дешевле серебра, но уже в древности это богатейшее месторождение было полностью истощено. Всего египтяне ко времени захвата Римом в 30 добыли около 6000 т золота. Огромные золотые богатства, находившиеся в погребениях фараонов, были почти все разграблены еще в древности.
В античные времена только из золотоносных пород Испании древние римляне добыли более 1500 тонн золота. И еще в середине 19 в. рудники Австро-Венгрии давали до 6,5 т золота в год, на некоторых золотых монетах того времени красуются надписи на латыни «Из золота Дуная», «Из золота Изара», «Из золота Инна» (притоки Дуная), «Из золота Рейна». Добыча в Финляндии исчислялась десятками килограммов в год. Сейчас золотые россыпи в долинах европейских рек практически полностью исчерпаны. После плаваний Колумба названная в его честь Колумбия длительное время занимала ведущее место в мире по добыче золота. Очень богатые золотоносные россыпи находили в 18–19 в. в Бразилии, США, Австралии, других странах.
В России своего золота долго не было. О начале его добычи мнения исследователей расходятся. По-видимому, первое отечественное золото было добыто в 1704 из Нерчинских руд вместе с серебром. В последующие десятилетия на Московском монетном дворе золото выделяли из серебра, которое содержало немного золота в виде примеси (около 0,4%). Так, в 1743–1744 «из золота, обретающегося в серебре, выплавленном на Нерчинских заводах», было изготовлено 2820 червонцев с изображением Елизаветы Петровны. Количество добытого золота было ничтожным: с 1719 по 1799 таким способом получили с огромными трудностями химического разделения всего 830 кг золота. По некоторым сведениям, небольшие количества золота (в 1745 – 6 кг) выплавили, причем тайно, на своих алтайских медных рудниках знаменитые Демидовы. С 1746 все эти рудники перешли в собственность царской семьи.
В 1745 на Урале было найдено коренное рудное золото, и в 1747 начал работать первый отечественный золотой рудник, названный впоследствии Первоначальным. За весь 18 в. в России было добыто всего лишь около 5 т золота, но уже в следующем столетии – в 400 раз больше. Открытие (в 1840-е) Енисейского месторождения вывело в те годы Россию на первое место в мире по добыче золота, но еще до этого местные охотники-эвенки делали из золотых самородков пули для охоты. В концу 19 в. Россия добывала в год около 40 т золота, из них 93% – россыпного. Всего же в России до 1917 было добыто по официальным данным 2754 т золота, но по оценкам специалистов – около 3000 т, причем максимум пришелся на 1913 (49 т), когда золотой запас достиг 1684.
Войны и революция привели к резкому спаду добычи золота. Так, в 1917 еще было добыто 28 т, а через три года – только 2,5 т, причем резко уменьшился и золотой запас – до 317 т (300 т вывезли в Германию по условиям Брестского мира, сотни тонн ушли с белой армией через Дальний Восток). Положение значительно улучшилось к концу 1920-х, после открытия в Восточной Сибири огромных запасов золота в бассейне реки Алдан в Якутии и на Колыме. В 1928 добыча золота достигла уже 28 т и продолжала неуклонно расти, достигнув в 302 т в 1990. После распада СССР Россия лишилась среднеазиатского золота, в том числе, крупнейшего месторождения в Узбекистане (оно стабильно давало около 60 т золота в год). В 1991 в России было добыто всего 168,1 т золота, причем добыча продолжала из года в год сокращаться, достигнув минимума в 1998 – 114,6 т. После этого она начала расти довольно быстрыми темпами: 1999 – 126,1 т, 2000 – 142,7 т, 2001 – 154,5 т, 2002 – 173,5 т, 2003 – 176,9 т. Основная часть добываемого золота уходит на экспорт, остальное идет в Гохран, в Центробанк, в промышленность (в том числе, в ювелирную). Добывают у нас золото в Магаданской, Читинской, Амурской областях, в Красноярском крае, в Якутии, на Чукотке.
Сейчас крупнейшим поставщиком золота на мировой рынок является Южная Африка, где шахты достигли уже 4-километровой глубины. В ЮАР находится самый большой в мире рудник Вааль-Рифс в Клексдорпе. При переработке 10 млн. тонн руды там извлекают примерно 80–90 тонн золота. Всего же в год в ЮАР добывают сотни тонн золота – около двух тонн ежедневно. Общие запасы золота в ЮАР оцениваются в 25 000 т. ЮАР – единственное государство, в котором золото – главный продукт производства, где золото добывают на 36 крупных рудниках, на которых трудятся сотни тысяч человек.
Однако золото, в отличие от нефти, не расходуется, а непрерывно накапливается, хотя в последние десятилетия и не так быстро (мировое производство достигло своего максимума в 1972). С другой стороны, разведанные его запасы ограничены, причем со временем разрабатываются все более бедные месторождения. Все это не может не отражаться (наряду с другими факторами) на цене золота. Цена же, в свою очередь, определяет рентабельность добычи. Падение цен на золото в последние два десятилетия 20 в. опасно приблизило продажную цену к себестоимости добычи, которая составляла к концу 20 в. около 220 долларов за тройскую унцию (31,1035 г) в США и 260 долларов в ЮАР (в ряде компаний – еще выше). Это привело к краху одних золотодобывающих компаний и снижению добычи другими. Так, если в 1970 в ЮАР было добыто 1004 т золота (пик добычи), то в 1975 – 713 т, в 1980 – 695 т, в 1985 – 673 т, в 2001 – только 399. А в Канаде и Австралии в период низких цен на золото его добыча даже дотировалась государством. В то же время при существенном повышении цены на золото разработка некоторых месторождений становится рентабельной. В ряде развивающихся стран себестоимость добычи оставалась сравнительно низкой (в Папуа – Новой Гвинее – 150 долларов за унцию), что позволяло им наращивать добычу. Годовое производство золота (в тоннах) в разные годы выглядела следующим образом:
| ГОДОВОЕ ПРОИЗВОДСТВО ЗОЛОТА (в тоннах) | ||||||
| Страна/год | 1913 | 1940 | 1960 | 1985 | 1999 | 2003 |
| ЮАР | 274 | 437 | 665 | 673 | 450 | 450 |
| США | 134 | 151 | 53 | 80 | 340 | 265 |
| Австралия | 69 | 51 | 34 | 59 | 303 | 275 |
| Китай | 171 | 175 | ||||
| Канада | 25 | 166 | 144 | 90 | 158 | 165 |
| Перу | 89 | 130 | 155 | |||
| Индонезия | 127 | 175 | ||||
| Россия | 49 | 126 | 177 | |||
| Узбекистан | 86 | 86 | ||||
| Гана | 80 | 174 | ||||
| Папуа – НоваяГвинея | 31 | 64 | ||||
| Бразилия | 5 | 6 | 72 | 54 | 78 | |
| Всего | 652 | 1138* | 1047* | 1233* | 2330 | 2500 |
| *Без СССР | ||||||
Сколько же всего добыто золота? И сколько его еще осталось? Учет (часто не вполне достоверный, особенно если золото добывается старателями) ведется со времени открытия Америки в конце 15 в. После плаваний Колумба испанские завоеватели в течение нескольких десятилетий привозили в Европу золото в таких количествах, что оно обесценилось в 5–6 раз. В 19 в. весь мир был потрясен «золотыми лихорадками» после открытия богатых залежей в Калифорнии (1848), в Австралии (1851), на Клондайке и Юконе на Аляске (1896 – 1900). «На золоте» выросли крупнейшие города – Сан-Франциско, Сидней, Йоханнесбург, а богатейшее в мире месторождение в Южной Африке, открытое в 1886 и содержащее около 30 г/т золота, не вызвало наплыва старателей-одиночек из-за особенностей его геологического строения: извлекать золото из твердых пород там можно было только с помощью специальной техники и тяжелейшего труда бесправного негритянского населения (в начале 20 в. на рудники было доставлено даже несколько десятков тысяч китайских рабочих).
На сегодня больше всего золота добыто в ЮАР – около 50 тысяч тонн, в России и СССР – более 14 тысяч, в США – более 10 тысяч (из них только в Калифорнии – 3500 т), немногим меньше в Канаде и в Австралии. Очень много золота (счет идет на тысячи тонн) добыто в Колумбии, Зимбабве, Гане, Мексике, Бразилии. Далее идут Филиппины, Заир и Перу. И во всех этих странах в месторождениях осталось меньше, чем уже добыто. Однако не все страны давали официальные сведения. Так, в СССР любая информация о золоте была засекречена, и имеющиеся сведения являются оценкой.
Общие итоги добычи золота таковы. За первые 4400 лет – с 3900 до н.э. (додинастический архаичный Египет) до 500 (падение Римской империи) – 10 000 т. За следующие 1000 лет (средневековье) – еще 2500 т. С начала 16 в. до начала 19 в. (340 лет) – 4900 т. Основная же масса добыта за последние 200 лет, а всего – порядка 130 тысяч тонн, причем примерно две трети – в течение последнего столетия (из них половина – в Южной Африке). Однако эти огромные количества – лишь сотые доли процента от объема стали, выплавляемой в мире только за один год. Собранное в одном месте, все это золото образовало бы куб с ребром, равным 19 м, то есть высотой с пятиэтажный дом (тогда как руда и песок, из которого это золото извлечено, представляло бы гору высотой более 2,5 км). В то же время золото, добываемое сейчас во всем мире за один год, поместилось бы в комнате средних размеров (правда, никакой пол такого груза не выдержит). Если можно было бы раздать золото, добытое за всю историю человечества, поровну между жителями Земли, каждый получил бы чуть больше 20 г, но такая операция невозможна даже теоретически: десятки тысяч тонн безвозвратно потеряны в результате истирания, захоронения в кладах, пошли на морское дно. Имеющееся же золото распределено так: около 10% в промышленных изделиях, остальное – приблизительно поровну между централизованными запасами (в основном, в виде стандартных слитков химически чистого золота), частными лицами и ювелирными изделиями.
Добыча золота: золотые самородки.
Наряду с маленькими крупинками в золотоносных районах изредка находят большие куски золота – самородки, которые всегда привлекают к себе внимание не только старателей. О крупных самородках пишут газеты, сообщают информационные агентства всего мира. Некогда очень богаты самородками были уральские месторождения. На сегодня во всем мире найдено примерно 10 тысяч самородков массой более 10 кг, и из них около 2 тысяч – только на территории Миасского района Челябинской Самый крупный – «Большой треугольник» размером 39 × 33 × 25,4 см и массой 36 кг 15,7 г – был найден в 1842 на Южном Урале (Царево-Александровский прииск), сейчас он хранится в Алмазном фонде. Еще через полвека на Урале нашли самородок массой 20 кг. Такие самородки представляют значительный интерес для ученых. Особенно редки хорошо ограненные кристаллы природного золота – сверкающие октаэдры, кубы, ромбододекаэдры и их комбинации. Иногда самородное золото образует красиво ветвящиеся веточки – дендриты.
В начале 19 в. был издан указ, согласно которому все более или менее крупные самородки (массой более 10–20 г) должны были поступать в музей Петербургского высшего горного училища, но с Урала хлынул такой поток золота, что в 1825 минимальная масса была повышена до 409 г (1 фунт). Но даже таких крупных самородков набралось столько, что поступил приказ большую их часть (свыше четверти тонны) сдать на монетный двор. Сохранившиеся самородки, в их числе и «Большой треугольник», составили основу Алмазного фонда. Сейчас даже не очень крупные самородки вряд ли будут переплавлять, потому что они представляют коллекционную ценность и стоят намного больше содержащегося в них золота.
Крупные самородки (обычно каждый из них имеет свое название) находили в России не только на Урале. В конце 19 в. в Иркутской области был найден самородок массой 22,6 кг, а в середине 20 в. на приисках вблизи населенных пунктов Бодайбо и Артемовский нашли несколько десятков крупных самородков массой до 10 кг и более. Очень богата самородками оказалась Колыма, где множество приисков. Уже во второй половине 20 в. там были найдены два самородка массой по 14 кг и сотни более мелких. Находили и продолжают находить большие самородки также в Якутии, в Хабаровском крае, на Алтае.
Среди зарубежных стран крупными самородками прославилась Австралия, где в середине 19 в. нашли несколько самородков массой 50 кг и более. Один из них, массой 70,9 кг (69,2 кг чистого золота) буквально валялся на дороге: в 1869 об него сломал колесо проезжавший по проселочной дороге экипаж. В Австралии в 1872 был найден и крупнейший в мире самородок – «Плита Холтермана» размером 140 × 66 × 10 см и массой 285,76 кг из золота, тесно сросшегося с кварцем, но для науки этот уникальный экземпляр был потерян: из него выплавили все золото, которого оказалось 93,3 кг. В конце 20 в. очень крупные самородки неожиданно нашли в Бразилии. А мелких самородков там находят в сумме более 10 тонн в год.
О более крупных самородках сохранились только сообщения древних авторов, которые трудно проверить. Так, аль Бируни в своей Минералогии упоминает найденный якобы в Афганистане самородок массой 2,5 тонны. По другим сведениям, на территории современной Чехии в 752 был найден самородок массой около 960 кг.
Применение золота.
Сейчас золото – прежде всего валютный металл, выполняющий функцию всеобщего эквивалента денег (см. ЗОЛОТО И ЭКОНОМИКА). Много золота оседает в банковских хранилища, еще больше используется для изготовления ювелирных изделий: на них расходуется более 70% слиткового металла. Ювелирная промышленность потребляет в год золота больше, чем его добывается: в 1990-е – 2300–2700 тонн ежегодно. При этом промышленно развитые страны потребляют только треть золота, а развивающиеся – 60%. Крупнейший потребитель золота – население Индии: в 2000 индийцы купили 1855 тонн драгоценного металла. Конечно, следует при этом учитывать и огромное население этой страны. Затем идут США (400–450 т в год), Саудовская Аравия (190–220 т), Китай и Турция (около 200 т); более 100 т в год потребляют страны Персидского залива, Южная Корея, Египет, Пакистан, Индонезия.
Золото расходуется также на изготовление монет и медалей, зубных протезов, коррозионноустойчивых деталей химических аппаратов, неокисляющихся электрических контактов, термопар, для нанесения защитных покрытий, изготовления специальных сортов стекла. Золото применяется при изготовлении деталей реактивных двигателей, ракет, ядерных реакторов, тепло- и светоотражающих покрытий космических аппаратов. В качестве катализатора золото (в виде контактной сетки) используется для окисления синильной кислоты до циановой, из которой получают полимеры и другие продукты. Сульфид цинка, активированный золотом, под воздействием пучка электронов светится зеленым цветом, что используется при изготовлении катодолюминофоров.
Применяется золото и в медицине. В 1583 французский алхимик, придворный врач и хирург Давид де Плани-Кампи опубликовал Трактат об истинном, непревзойденном, великом и универсальном лекарстве древних, или же о питьевом золоте, несравненной сокровищнице неисчерпаемых богатств. В нем он, ссылаясь на своих предшественников, в основном, арабских алхимиков, описывал целебные свойства так называемого питьевого золота, приписывая ему самые чудодейственные свойства. Уповал на aurum potabile (питьевое золото) и знаменитый врач-алхимик 16 в. Филипп Ауреол Теофраст Бомбаст фон Гогенгейм, более известный под именем Парацельса. Это и было золото в буквальном смысле этого слова, только очень мелко раздробленное – коллоидный раствор золота красного цвета. О питьевом золоте упоминают и китайские книги по медицине, датированные I в. до н.э. Китайские врачи подразумевали под этим названием «эликсир жизни» – напиток, дарующий молодость, здоровье и силу. Сейчас установлено, что золото, как и серебро, обладает бактерицидными свойствами.
В конце 19 в. немецкий микробиолог Роберт Кох обнаружил, что тетрацианоаурат(III) калия K[Au(CN)4] прекращает рост туберкулезных бактерий. В 20 веке препараты золота, например, тиосульфатный комплекс санокризин Na3[Au(S2O3)2]·2H2O, начали применять для лечения туберкулеза, артрита, как противовоспалительное средство. Сейчас для лечения ревматоидного артрита применяют препарат кризанол, содержащий 33,5% золота в виде ауротиопропанолсульфоната кальция (AuSCH2CH(OH)CH2SO3)2Ca, и ауранофин, также содержащий связь Au–S и координационной связанный с атомом золота триэтилфосфин:
R–S–Au ¬ P(C2H5)3, где R – полностью ацетилированный остаток глюкозы. Предполагается, что препараты золота влияют на иммунные процессы в организме. В радиотерапии используют радионуклид 198Au с периодом полураспада около 3 суток.
Высокая плотность золота иногда приводит к его необычному применению. В начале 1990-х на киностудии Центрнаучфильм снимался научно-популярный фильм о золоте. Автор сценария и оператор Евгений Георгиевич Покровский в поиске интересных сюжетов побывал в Алмазном фонде в Московском Кремле, там его внимание привлек находящийся в витрине шар из золота. Сотрудник фонда сказал, что шар этот весит два пуда и сделан он по заказу Д.И.Менделеева. Однако с какой целью изготовлен шар, он сказать не мог. Пришлось кинооператору обратиться за помощью к консультанту.
Выяснилось, что Положением Государственного совета Российской Империи 8 июня 1863 в Петербурге было учреждено Депо образцовых мер и весов. В 1892 министр финансов С.Ю.Витте предложил Д.И.Менделееву занять пост ученого хранителя мер и весов в Депо. Менделеев принял предложение и энергично взялся за новое для него дело. Вскоре Депо было преобразовано в Главную палату мер и весов; Менделеев оставался ее управляющим в течение последних 15 лет своей жизни. За эти годы им были выполнены важные исследования в области метрологии – отрасли физики, задачей которой является создание эталонов физических единиц и разработка методик точных измерений. Под руководством Менделеева были изготовлены российские эталоны метра, литра, килограмма, а также старых мер – фунта, аршина и др. Целью Менделеева был переход страны на метрическую систему мер, что было осуществлено лишь в 1918.
Для проведения в Палате точных измерений ускорения свободного падения на широте Петербурга нужно было с высокой точностью измерить период колебаний маятника известной длины, поскольку длина маятника, период его колебаний и ускорение силы тяжести связаны простым соотношением. Но точно оно выполняется только для идеального (математического) маятника, у которого размах колебаний небольшой, нить невесома, груз – точечный, а сопротивление воздуха отсутствует. Чтобы реальный маятник был близок к идеальному, он должен быть изготовлен из тяжелого материала и подвешен на длинной тонкой нити. Вот Менделеев и решил в качестве груза для маятника использовать тяжелое золото. По его заказу был изготовлен массивный полированный (для уменьшения сопротивления воздуха) золотой шар. При массе 2 пуда (32 кг) его радиус был равен всего 7,3 см. Поскольку в здании Палаты не было высоких залов, Менделеев, чтобы удлинить нить подвеса, приказал пробить перекрытия на нескольких этажах, да еще выкопать яму в подвале. С помощью такого маятника можно было измерить ускорение силы тяжести с высокой точностью.
Золото

Золото — минерал, являющийся природным твёрдым раствором серебра (следы, до 43%) в золоте; обычны примеси (следы, до 0,9%) меди, железа, свинца, реже – висмута, ртути, платины, марганца и др. Известны разновидности с повышенным содержанием меди – до 20% (медистое золото, купроаурит), висмута – до 4% (висмутистое золото, висмутаурит), платиноидов (платинистое и иридистое золото; порпецит – Au, Pd, родит – Au, Rh), природные амальгамы (Au, Hg).
СТРУКТУРА
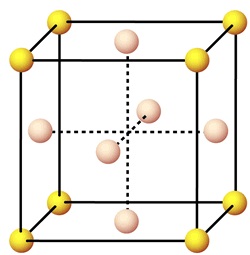
Кристаллическая структура золота
Кристаллизуется в кубической сингонии, в виде октаэдров, ромбододекаэдров, кубов и более сложных по форме кристаллов; нередко они искажены, сильно вытянуты, образуя “проволочки”, “волоски”, или уплощены параллельно грани октаэдра. Для самородного золота особенно низкопробного, характерно многообразие форм роста, оно обычно в виде скелетных кристаллов, дендритов, нитевидных и скрученно-нитевидных кристаллов. Широко распространены прожилковидные и неправильные комковидные, “крючковатые” выделения; на их поверхности нередко сохраняются отпечатки кристаллов других минералов, агрегаты которых включали скопления самородного золота. Травление выявляет кристаллически-зернистое строение золотых частиц.
СВОЙСТВА

Золотые слитки и самородки
Золото — очень тяжёлый металл: плотность чистого золота равна 19,32 г/см³ (шар из чистого золота диаметром 46,237 мм имеет массу 1 кг). Диамагнетик, то есть, магнитное поле в золоте ослабевает. Среди металлов по плотности занимает седьмое место после осмия, иридия, рения, платины, нептуния и плутония. Сопоставимую с золотом плотность имеет вольфрам (19,25). Высокая плотность золота облегчает его добычу, отчего даже простые технологические процессы — например, промывка на шлюзах, — могут обеспечить высокую степень извлечения золота из промываемой породы.
Золото — очень мягкий металл: твёрдость по шкале Мооса ~2,5, по Бринеллю 220—250 МПа (сравнима с твёрдостью ногтя).
Золото также высокопластично: оно может быть проковано в листки толщиной до ~0,1 мкм (100 нм) (сусальное золото); при такой толщине золото полупрозрачно и в отражённом свете имеет жёлтый цвет, в проходящем — окрашено в дополнительный к жёлтому синевато-зеленоватый. Золото может быть вытянуто в проволоку с линейной плотностью до 2 мг/м.
Температура плавления золота 1064,18 °C (1337,33 К), кипит при 2856 °C (3129 К). Плотность жидкого золота меньше, чем твёрдого, и составляет 17 г/см 3 при температуре плавления. Жидкое золото довольно летучее, и активно испаряется задолго до температуры кипения.
ЗАПАСЫ И ДОБЫЧА

Содержание золота в земной коре очень низкое — 4,3·10 -10 % по массе (0,5-5 мг/т), но месторождения и участки, резко обогащённые металлом, весьма многочисленны. Золото содержится и в воде. Один литр и морской, и речной воды содержит менее 5·10 −9 граммов Au, что примерно соответствует 5 килограммам золота в 1 кубическом километре воды.
Золоторудные месторождения возникают преимущественно в районах развития гранитоидов, небольшое их количество ассоциирует с основными и ультраосновными породами.
Для получения золота используются его основные физические и химические свойства: присутствие в природе в самородном состоянии, способность реагировать лишь с немногими веществами (ртуть, цианиды). С развитием современных технологий более популярными становятся химические способы.
В 1947 году американские физики Ингрем, Гесс и Гайдн проводили эксперимент по измерению эффективного сечения поглощения нейтронов ядрами ртути. В качестве побочного эффекта эксперимента было получено около 35 мкг золота. Таким образом, была осуществлена многовековая мечта алхимиков — трансмутация ртути в золото. Однако экономического значения такое производство золота не имеет, так как обходится во много раз дороже добычи золота из самых бедных руд.
ПРОИСХОЖДЕНИЕ

Изделия из золота
Самородное золото – главная форма нахождения золота в природе. Оно концентрируется в гидротермальных месторождениях образуя золотые руды, неравномерно распределяясь в трещиноватом жильном кварце и в сульфидах – пирите, арсенопирите, пирротине и др. В существенно сульфидных рудах самородное золото тонкодисперсное. При окислении руд на земной поверхности мелкое самородное золото частично растворяется и переотлагается; в ряде случаев оно обогащает верхние части рудных тел. Процессы их разрушения приводят к освобождению частиц самородного золота и их накоплению в россыпях; перемещаясь водными потоками вместе с другим кластическим материалом, частицы окатываются, округляются, деформируются, частично перекристаллизовываются; в результате электрохимической коррозии на них образуется тонкая оболочка высокопробного золота, что приводит к общему повышению пробы самородного золота в россыпях.
ПРИМЕНЕНИЕ

По своей химической стойкости и механической прочности золото уступает большинству платиноидов, но незаменимо как материал для электрических контактов. Поэтому в микроэлектронике золотые проводники и гальванические покрытия золотом контактных поверхностей, разъёмов, печатных плат используются очень широко.
Золото используется в качестве мишени в ядерных исследованиях, в качестве покрытия зеркал, работающих в дальнем инфракрасном диапазоне, в качестве специальной оболочки в нейтронной бомбе. Тонкий слой золота (20 нм) на внутренней поверхности оконных и витражных стекол существенно уменьшает нежелательные тепловые потери зимой, а летом предохраняет внутренние помещения зданий и транспортных средств от нагревания инфракрасными лучами.
Золотые припои очень хорошо смачивают различные металлические поверхности и применяются при пайке металлов. Тонкие прокладки, изготовленные из мягких сплавов золота, используются в технике сверхвысокого вакуума.
Традиционным и самым крупным потребителем золота является ювелирная промышленность. Ювелирные изделия изготавливают не из чистого золота, а из его сплавов с другими металлами, значительно превосходящими золото по механической прочности и стойкости. В настоящее время для этого служат сплавы Au-Ag-Cu, которые могут содержать добавки цинка, никеля, кобальта, палладия. Стойкость к коррозии таких сплавов определяются, в основном, содержанием в них золота, а цветовые оттенки и механические свойства — соотношением серебра и меди.
Значительные количества золота потребляет стоматология: коронки и зубные протезы изготовляют из сплавов золота с серебром, медью, никелем, платиной, цинком. Такие сплавы сочетают коррозионную стойкость с высокими механическими свойствами.
Соединения золота входят в состав некоторых медицинских препаратов, используемых для лечения ряда заболеваний (туберкулёза, ревматоидных артритов и т. д.). Радиоактивный изотоп 198 Au (период полураспада 2,967 сут.) используется при лечении злокачественных опухолей в радиотерапии.
Источник https://stone-stream.ru/metally/chto-tyazhelee-zoloto-ili-zhelezo.html
Источник https://www.krugosvet.ru/enc/nauka_i_tehnika/himiya/ZOLOTO.html
Источник https://mineralpro.ru/minerals/gold/





